Säure- Base Reaktionen
Wir betrachten dabei nichts weiter als die reaktion zweier
korrespondierender Säure -Base Paare! Für beide Teilsysteme kann man
die 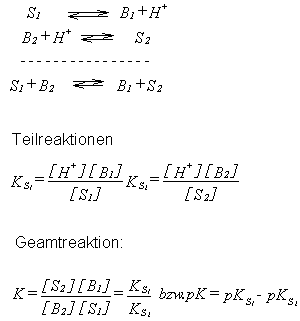 Säurekonstante definieren (sprich das MWG der jeweiligen
Teilreaktion). Das sich dabei einstellende Gleichgewicht ist durch eine
bestimmte Wasserstoffionenkonzentration bestimmt.
Säurekonstante definieren (sprich das MWG der jeweiligen
Teilreaktion). Das sich dabei einstellende Gleichgewicht ist durch eine
bestimmte Wasserstoffionenkonzentration bestimmt.
Für die Gesamtreaktion folgt dann die Gleichung, wie rechts
beschrieben.Zur Beschreibung der Lage des Gleichgewichtes kann man
folgendes sagen:
Das Gleichgewicht liegt um so mehr auf der rechten Seite, je größer KS1
gegenüber KS2 ist.
Das Gleichgewicht der Reaktion einer Säure mit einer Base liegt um so
mehr auf der Seite der Reaktionsprodukte, je stärkere Säuren und Basen
die Ausgangsstoffe sind.
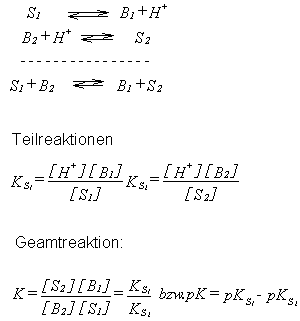 Säurekonstante definieren (sprich das MWG der jeweiligen
Teilreaktion). Das sich dabei einstellende Gleichgewicht ist durch eine
bestimmte Wasserstoffionenkonzentration bestimmt.
Säurekonstante definieren (sprich das MWG der jeweiligen
Teilreaktion). Das sich dabei einstellende Gleichgewicht ist durch eine
bestimmte Wasserstoffionenkonzentration bestimmt.